http://www.focus.de/panorama/videos/koerper-eines-hirntoten-spenders-erste-kopf-transplantation-am-menschen-dieser-russe-meldet-sich-freiwillig_id_4603163.html
Pop Culture
https://www.pinterest.com/clineltolf/posthumanism/
Mapping Posthumanismus
Bodyhackingcon
Bodyhackers come in all shapes, sizes, and colors. Even “normal” ones. That’s because bodyhacking isn’t just about appearances. It can relate to inward reflection, chemical adjustment, or even a fancy new watch that connects to a smartphone. The body is a vehicle to be tuned, modified, added to, taken away from, painted, tweaked, and customized.
Entdeckung CRISPR/Cas-Methode
Die Entdeckung und Erforschung der CRISPR-Sequenzen und des damit verbundenen CRISPR/Cas-Systems im Immunsystem verschiedener Bakterien und Archaea erfolgte in mehreren Schritten seit den späten 1980er Jahren. Vor allem in den frühen 2000ern wurden die Zusammenhänge zwischen den CRISPR-Sequenzen der DNA und den cas-Genen sowie ihre Bedeutung in der Immunabwehr der Bakterien identifiziert.
Im Jahr 2011 zeigte eine Arbeitsgruppe um Emmanuelle Charpentier und Jennifer Doudna, dass mithilfe des CRISPR/Cas-Systems der Mikroorganismen spezifische DNA-Ziele in vitro geschnitten werden können. Sie reichten ihre wissenschaftliche Arbeit am 8. Juni 2012 bei der Fachzeitschrift Science ein, wo sie am 28. Juni veröffentlicht wurde. Parallel zu ihnen arbeitete eine Arbeitsgruppe um Virginijus Šikšnys an der Methode, die bereits im April 2012 ihre Arbeit bei Cell einreichten, diese wurde jedoch abgelehnt, wenngleich die Herausgeber von Cell dem Artikel nachträglich eine große Bedeutung zuschrieben. Im Mai reichten Šikšnys und Kollegen das Papier in den Proceedings of the National Academy of Sciences (PNAS) ein, wo es am 4. September online veröffentlicht wurde.
Doudna und Charpentier beschrieben, wie sich in einem Bakterium gezielt Abschnitte aus dem Erbgut entfernen lassen. Dem Neurowissenschaftler Feng Zhang vom Massachusetts Institute of Technology gelang es später, die CRISPR-Methode nicht nur im Bakterium anzuwenden, sondern für alle Zellen zu optimieren. Der Leiter des Broad Institute und Vorgesetzte von Feng Zhang, Eric Lander, verfasste im Januar 2016 einen Artikel über die Anteile der verschiedenen Wissenschaftler an der Entdeckung des CRISPR/Cas-Systems, der aufgrund von einseitiger Darstellung und eines vermuteten Interessenskonflikts kritisiert wurde.
Charpentier und Doudna erhielten 2014 für die Entdeckung der CRISPR/Cas-Methode den mit drei Millionen Dollar für jeden Preisträger dotierten Breakthrough Prize in Life Sciences und wurden mit zahlreichen weiteren Preisen bedacht.
Designer-Baby?
01. Februar 2016
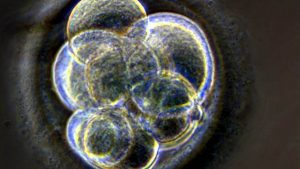
Ein Team um Kathy Niakan vom Francis-Crick-Institut in London will das Erbgut menschlicher Embryonen verändern. Dafür haben die Forscher bei der zuständigen britischen Regulierungsbehörde HFEA (Human Fertilisation and Embryology Authority) einen Antrag gestellt. Dieser wurde nun genehmigt.
Die Wissenschaftler wollen mit Embryonen forschen, die bei künstlichen Befruchtungen übrig geblieben sind und von den Paaren gespendet wurden. Sieben Tage nach der Befruchtung sollen die Versuche gestoppt, die manipulierten Embryonen entsorgt werden. Den Wissenschaftlern ist es verboten, einen Embryo mit verändertem Erbgut in die Gebärmutter einzupflanzen. Es geht um Grundlagenforschung, nicht um Therapie.
Kathy Niakan zufolge könnten die Forscher in den nächsten Monaten loslegen. Allerdings steht noch die Zustimmung einer Ethikkommission aus.
Wie greifen die Forscher ins embryonale Erbgut ein?
Sie verwenden dafür ein relativ neues Verfahren: CRISPR/Cas9. Mithilfe dieser auch als Genchirurgie bezeichneten Methode, lassen sich Gene aus dem Erbgut relativ einfach und präzise herausschneiden oder einfügen.
Die Methode wird weltweit in vielen Laboren genutzt, ihre Erfinder – darunter die Forscherin Emmanuelle Charpentier, Direktorin am Berliner Max-Planck-Institut für Infektionsbiologie – gelten als heiße Kandidaten für den Nobelpreis. Das Verfahren kommt in ganz unterschiedlichen Bereichen zum Einsatz: So versuchen Forscher etwa, menschliche Abwehrzellen so zu verändern, dass sie dem HI-Virus kein Einfalltor mehr bieten. Auch Pflanzen, die immun gegen Schädlinge sind, lassen sich so züchten.
Die Technik macht es allerdings auch möglich, menschliche Keimzellen und Embryonen zu manipulieren, was ethisch heftig umstritten ist. Kathy Niakan und ihr Team wollen in einem ersten Versuch ein Gen namens OCT4 blockieren. Dieses spielt eine wichtige Rolle bei der Entwicklung von pluripotenten Zellen: Es entscheidet vermutlich, welche Zellen den Embryo und welche die Plazenta bilden.
Warum greifen die Forscher ins Erbgut von Embryonen ein?
Die Londoner Forscher wollen besser verstehen, wie der Beginn des Lebens abläuft und welche Gene es braucht, damit sich ein Embryo gesund entwickelt. Denn der Prozess ist extrem störanfällig.
Nach den sieben Tagen, die Kathy Niakan und ihr Team die befruchteten Eizellen beobachten wollen, haben diese das sogenannte Blastozysten-Stadium erreicht. Sie bestehen dann aus bis zu 256 Zellen. Doch selbst dieses frühe Stadium der Entwicklung schaffen längst nicht alle befruchteten Eizellen: von etwa hundert entwickelt sich weniger als die Hälfte so weit.
Fehlgeburten und Unfruchtbarkeit seien relativ häufig, doch die Gründe dafür seien bis jetzt noch nicht ausreichend verstanden, sagte Niakan der BBC. Mit ihrer Forschung will sie das Verständnis für die Ursachen verbessern.
Warum ist der Eingriff am Erbgut von Embryonen umstritten?
Kritiker warnen, dass die Technik den Weg zu Designerbabys ebnet. Auch Krankheiten könnten theoretisch beseitigt werden, bevor sie entstehen. Doch davon ist die Realität noch weit entfernt. Zwar sorgten chinesische Wissenschaftler für einen Eklat und hitzige Diskussionen, als sie im vergangenen Jahr bekannt gaben, dass sie zum ersten Mal das Erbgut von Embryonen verändert hatten. Eine Grenze sei damit überschritten, urteilten viele Forscher. Sie forderten eine Debatte darüber, wie weit die Wissenschaft gehen will und darf.
Doch es zeigte sich auch: Die Technik ist noch lange nicht ausgereift. Für ihren Versuch verwendeten die Chinesen 86 nicht entwicklungsfähige Embryos. Bei diesen versuchten sie, ein Gen zu reparieren, das zu der schweren Blutkrankheit Thalassämie führt. Doch das klappte nur in vier Fällen. Zudem fanden sich – häufiger als aus Versuchen mit erwachsenen menschlichen Zellen bekannt – unbeabsichtigte Veränderungen des Erbguts. An menschlichen Embryonen funktioniert CRISPR/Cas9 offenbar nicht so präzise.
Neben den ethischen Bedenken wirft das allerdings die Frage auf, wie sicher die Technik ist: Forscher befürchten, dass der Mensch am Erbgut herumschnippelt und Dinge verändert, die er gar nicht verändern will. Manipulationen an Keimzellen betreffen zudem nicht nur den jeweiligen Embryo, sie werden auch an die Nachkommen weitergegeben. Die Technik an Keimzellen anzuwenden, sei daher „gefährlich und ethisch inakzeptabel“, schreiben Forscher in einem Kommentar in „Nature News“.
In einem Statement, das die führenden Experten im Dezember herausgegeben haben, heißt es allerdings: Grundlagenforschung sei auch in diesem Bereich notwendig und solle stattfinden. Allerdings dürften die manipulierten Embryonen nicht dazu verwendet werden, eine Schwangerschaft herbeizuführen.
Der deutsche Experte Prof. Hans Schöler bewertet die Entwicklung mit Skepsis: „Diese Forschung hat eine neue Qualität. Sie öffnet eine Tür, gezielt in die Keimbahn eines menschlichen Embryos einzugreifen“, sagte der Leiter des Max-Planck-Instituts für molekulare Biomedizin in Münster der Deutschen Presse-Agentur. „Dass solche Eingriffe nicht durchgeführt werden, war bislang internationaler Konsens. Die Briten wollen offenbar eine Vorreiterrolle einnehmen.“
Wäre so etwas auch in Deutschland möglich?
Nein. Das Embryonenschutzgesetz verbietet hierzulande Experimente wie das der Londoner Forscher. Doch weltweit ist die Gesetzeslage alles andere als einheitlich: In Ländern wie China, Japan, Indien oder auch Irland gibt es keine verbindlichen Vorschriften für die Genmanipulation an Embryonen, schreibt „Nature News“. Viele Wissenschaftler würden sich daher zumindest international gültige Richtlinien wünschen.
Denn während noch über Grundsätzliches diskutiert wird, preschen Forscher wie Kathy Niakan vom Francis-Crick-Institut in London vor. Sie könnten ihrem Fachgebiet dadurch auch enormen Schaden zufügen: Gerät die Genchirurgie durch Berichte über die Manipulation an Embryonen als Frankenstein-Technik in Verruf, könnte auch die Akzeptanz für ihren Einsatz an menschlichen Zellen sinken, befürchten Forscher. Das würde die Suche nach neuen Therapien gegen HIV oder Krebs behindern.
Gentechnisch veränderte Organismen (GVO), auch gentechnisch modifizierte Organismen (genetically modified organism GMO) sind Organismen, deren Erbanlagen mittels gentechnischer Methoden (z. B. durch Transgenetik) gezielt verändert worden sind.
Zur Genmodifikation zählen die gezielte Abschaltung einzelner Gene sowie das gezielte Einbringen arteigener oder artfremder Gene. GVOs, in die Gene aus anderen Arten eingeschleust wurden, werden auch als transgene Organismen bezeichnet, die eingeschleusten Gene als Transgene. So werden beispielsweise Gene zwischen verschiedenen Arten übertragen, um Tieren oder Pflanzen bestimmte Eigenschaften zu vermitteln, die mit herkömmlicher Züchtung nicht oder schwerer zu erreichen wären.
genetisch veränderte Organismen
Definition Posthumanismus
Posthumanismus ist eine Philosophie, die eine Überwindung des gegenwärtigen menschlichen Stadiums anstrebt. Sie ist eng mit der Denkrichtung des Transhumanismus verknüpft.
(https://de.wikipedia.org/wiki/Posthumanismus#Posthumanismus)
Hallo Welt!
Willkommen zu blog.zhdk.ch. Das ist Dein erster Eintrag. Ändere oder lösche in und starte mit Deinem Blog!